L’axe 1 associe des études biocliniques et épidémiologiques de type EXPOSOME sur cohortes pour identifier les facteurs environnementaux et individuels de progression (expositions, comorbidités, facteurs socio-économiques), et des études de modélisation du processus pulmonaire fibrosant à partir d’images tomodensitométriques et de données physiologiques. Les principales réalisations et les projets en cours sont les suivants :
Identification des facteurs associés à la sévérité et à la progression des PID :
Impact des facteurs environnementaux (pollution atmosphérique, expositions professionnelles) et socio-économiques :
- Sesé L et al. Role of atmospheric pollution on the natural history of idiopathic pulmonary fibrosis. Thorax. 2018 Feb;73(2):145-150. PMID: 28798214
- Sesé et al. Gender Differences in Idiopathic Pulmonary Fibrosis: Are Men and Women Equal? Front Med (Lausanne). 2021 Aug 5;8:713698. PMID: 34422868.
- Sesé et al. Low income and outcome in idiopathic pulmonary fibrosis: An association to uncover. Respir Med. 2021 Jul;183:106415. PMID: 33965849.
- Sesé et al. Impact of socioeconomic status in patients hospitalised for COVID-19 in the Greater Paris area. Eur Respir J. 2020 Dec 24;56(6):2002364. PMID: 33154032.
- Uzunhan et al. Chronic pulmonary aspergillosis complicating sarcoidosis. Eur Respir J. 2017 Jun 15;49(6):1602396. PMID: 28619957.
Rôle des comorbidités : apnées du sommeil et hypoxie intermittente nocturne
- Gille et al. Obstructive sleep apnoea and related comorbidities in incident idiopathic pulmonary fibrosis. Eur Respir J. 2017 Jun 8;49(6):1601934. PMID: 28596432.
Etudes en cours :
- « EXPOSOM-FPI: Rôle des facteurs socio-économiques et environnementaux dans l’histoire naturelle de la FPI » 2019-2023 (# ANSES-19-EST-241). Coordinateurs : L Sesé & H Nunes (H&P)
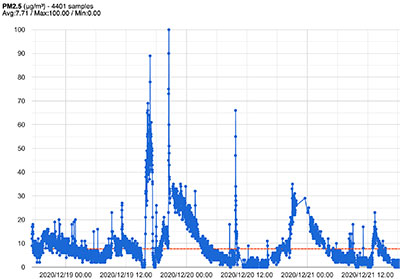
- « OBIWAN-FPI : Objets connectés pour mesurer l’impact de la pollution atmosphérique sur l’évolution de la fonction respiratoire de la fibrose pulmonaire idiopathique ». Coordinatrice : L Sesé (H&P). Recherche participative en collaboration avec l’AFPF (Association Fibroses Pulmonaires France)
- « NUTRINET-FPI: Influence de l’alimentation sur le pronostic de la fibrose pulmonaire idiopathique ». Coordinatrice : L Sesé (H&P)
- « NUTRISARC: Influence de la nutrition sur le développement et le pronostic de la sarcoïdose ». Coordinatrice : F Jeny (H&P)
Prises en charge et thérapeutiques innovantes dans les PID sévères :
Scores diagnostiques et facteurs prédictifs de mortalité dans la sarcoïdose pulmonaire fibrosante :
- Jeny et al. Validation of the Sarcoidosis Diagnostic Score (SDS) in a Multicontinental Study. Ann Am Thorac Soc. 2022 Nov 2. doi: 10.1513/AnnalsATS.202206-529OC. PMID: 36322428.
- Jeny et al. Predictors of mortality in fibrosing pulmonary sarcoidosis. Respir Med. 2020 Aug;169:105997. PMID: 32442108.
Efficacité des inhibiteurs de la JAK dans la sarcoïdose réfractaire :
- Rotenberg et al. Dramatic response of refractory sarcoidosis under ruxolitinib in a patient with associated JAK2-mutated polycythemia. Eur Respir J. 2018 20;52(6):1801482. PMID: 30361243.
Recommandations internationales de prise en charge clinique de la sarcoïdose :
- Baughman RP, Valeyre D et al. ERS clinical practice guidelines on treatment of sarcoidosis. Eur Respir J. 2021 17:2004079. PMID: 34140301. D Valeyre : co-chairman de la task force
Traitement des exacerbations aiguës de FPI par l’association cyclophosphamide et glucocorticoïdes (PHRC EXAFIP I)
- Naccache JM, …, Nunes H. Cyclophosphamide added to glucocorticoids in acute exacerbation of idiopathic pulmonary fibrosis (EXAFIP): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Respir Med. 2022;10(1):26-34. PMID: 34506761.
Etudes en cours :
- « PALIF: Impact sur la qualité de vie d’une prise en charge palliative systématique dans la fibrose pulmonaire idiopathique ». PHRC #NCT03229343. 2017-2022. Coordinateur : B Duchemann (H&P)
- « QUIDOSE: Essai randomisé contrôlé testant l'efficacité de l'hydroxychloroquine associée à une corticothérapie faible dose dans la sarcoïdose pulmonaire ». PHRC #NCT05247554. 2020-2023. Coordinatrice : F Jeny (H&P)
- « EXAFIP II : Intérêt du cyclophosphamide associé aux corticostéroïdes dans le traitement des EXacerbations Aiguës de FIbrose Pulmonaire idiopathique ». PHRC #NCT02460588 Coordinateur: JM Naccache. Président du Comité Scientifique: H Nunes (H&P)
Imagerie et modélisation multi-échelle du poumon fibreux :
Intérêt de la Minimal Intensity Projection pour le diagnostic de FPI
- De Margerie-Mellon et al. Computed tomography assessment of peripheral traction bronchiolectasis: impact of minimal intensity projection. Eur Respir J. 2020 Jan 23;55(1):1901388. PMID:31649065.
Imagerie innovante pour l’estimation des séquelles de pneumonie COVID-19 :
- « SILICOVILUNG : modélisation in silico du TDM thoracique et séquelles du COVID-19 » ANR RA COVID-19 2020 (ANR#20-COV4-0004, clinical trial #NCT04747769). Coordinateur : PY Brillet (H&P)
- Fetita C, …, Gille T, Nunes H, Bernaudin JF, Brillet PY. "Multiparameter analysis of vascular remodeling in post-acute sequelae of COVID-19," Proc. SPIE 12033, Medical Imaging 2022: Computer-Aided Diagnosis, 120330A (4 April 2022); https://doi.org/10.1117/12.2611461
Analyse multicompartimentale de l’imagerie pulmonaire :
- « LungManyScale: computational LUNG biomechanics: MANY-SCALE modeling and estimation » (ANR#19-CE45-43007) (2019-2022). Coordinateur : M Genet (M3DISIM-Laboratoire de Biomécanique des Solides, Ecole Polytechnique/Institut Polytechnique de Paris); partenaire : PY Brillet (H&P)
- Patte C, Brillet PY, Fetita C, Bernaudin JF, Gille T, Nunes H, Chapelle D, Genet M. Estimation of Regional Pulmonary Compliance in Idiopathic Pulmonary Fibrosis Based on Personalized Lung Poromechanical Modeling. J Biomech Eng. 2022;144(9):091008. PMID: 35292805.
- Laville, C., Fetita, C., Gille, T., Brillet, P.-Y., Nunes, H., Bernaudin, J.-F. & Genet, M. (2023). Comparison of optimization parametrizations for regional lung compliance estimation using personalized pulmonary poromechanical modeling. Biomech Model Mechanobiol. 2023;13:1-13
- Brevet # FR2305932 "Estimation non invasive in vivo de paramètres constitutifs de tissus mous et de paramètres de chargement à partir d’images biomédicales" PY Brillet (UMR1272 H&P) co-inventeur (juin 2023)
Etude en cours :
- « MLQ-CT: Multicompartmental lung quantitative computed tomography MLQ-CT » ANR Translationnelle en Santé CE-17 2023-2026. Coordinateur : PY Brillet (H&P)